GMP纯化水系统药典标准有哪些?
与2015版《中国药典》相比,2020版《中国药典》标准体系进一步完善,在制药用水方面始终保持严苛要求,纯化水与注射用水的强制项下指标中包括性状、酸碱度、硝酸盐、亚硝酸、氨盐、电导率、总有机碳、易氧化物、不挥发物、重金属、微生物限度,注射用水的制备原水仍维持为纯化水,并且制备工艺维持为只允许蒸馏法。
GMP纯化水系统药典标准有哪些?国家对医疗用纯化水水质和注射用水水质有严格的法律条文要求。根据《医疗器械生产质量管理规范》规定:对于直接或间接接触心血管系统、淋巴系统或脑脊髓液或药液的无菌医疗器械,若水是最终产品的组成成分时,应当使用符合《中国药典》要求的注射用水;若用于末道清洗应当使用符合《中国药典》要求的注射用水或用超滤等其他方法产生的同等要求的注射用水。与人体组织、骨腔或自然腔体接触的无菌医疗器械,末道清洗用水应当使用符合《中国药典》要求的纯化水。
依据《无菌医疗器具生产》(YY0033-2000)标准的规定:设备、工装上与产品直接接触的部位及工作台面、工位器具应定期清洗、消毒、保持清洁、洁净区(室)内的工位器具应在洁净区(室)内用纯化水进行清洗、消毒。
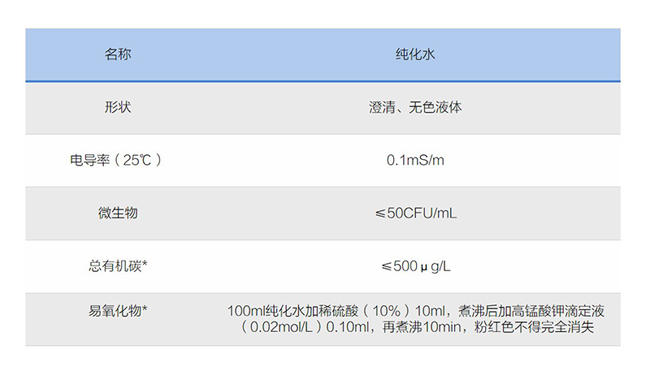
由国家食品药品监管总局发布的《YYT 1244-2014 体外诊断试剂用纯化水》,明确指出了医药行业中体外诊断试剂对于纯化水的要求,用纯水电导率(25℃)≤0.1mS/m,微生物总数≤50CFU/mL,总有机碳≤500μg/L,易氧化物100ml纯化水加稀硫酸(10%)10ml,煮沸后加高锰酸钾滴定液(0.02mol/L)0.10ml,再煮沸10min,粉红色不得完全消失。
综上可以看出,伴随2020版《中国药典》的颁布,未来监管力度会越来越大,这意味着制药企业将面临着新一轮实验室质量体系提升的挑战。
新闻标题:GMP纯化水系统药典标准有哪些?
网页URL:https://www.cdcxhl.com/hangye/chunshuiji/n11381.html
声明:本网站发布的内容(图片、视频和文字)以用户投稿、用户转载内容为主,如果涉及侵权请尽快告知,我们将会在第一时间删除。文章观点不代表本网站立场,如需处理请联系客服。电话:028-86922220;邮箱:631063699@qq.com。内容未经允许不得转载,或转载时需注明来源: 创新互联
纯水机相关推荐

我想展现纯水机信息
加入纯水机信息推广
免费获取纯水机推广方案
- 姓名:
- 电话:
- 需求:


